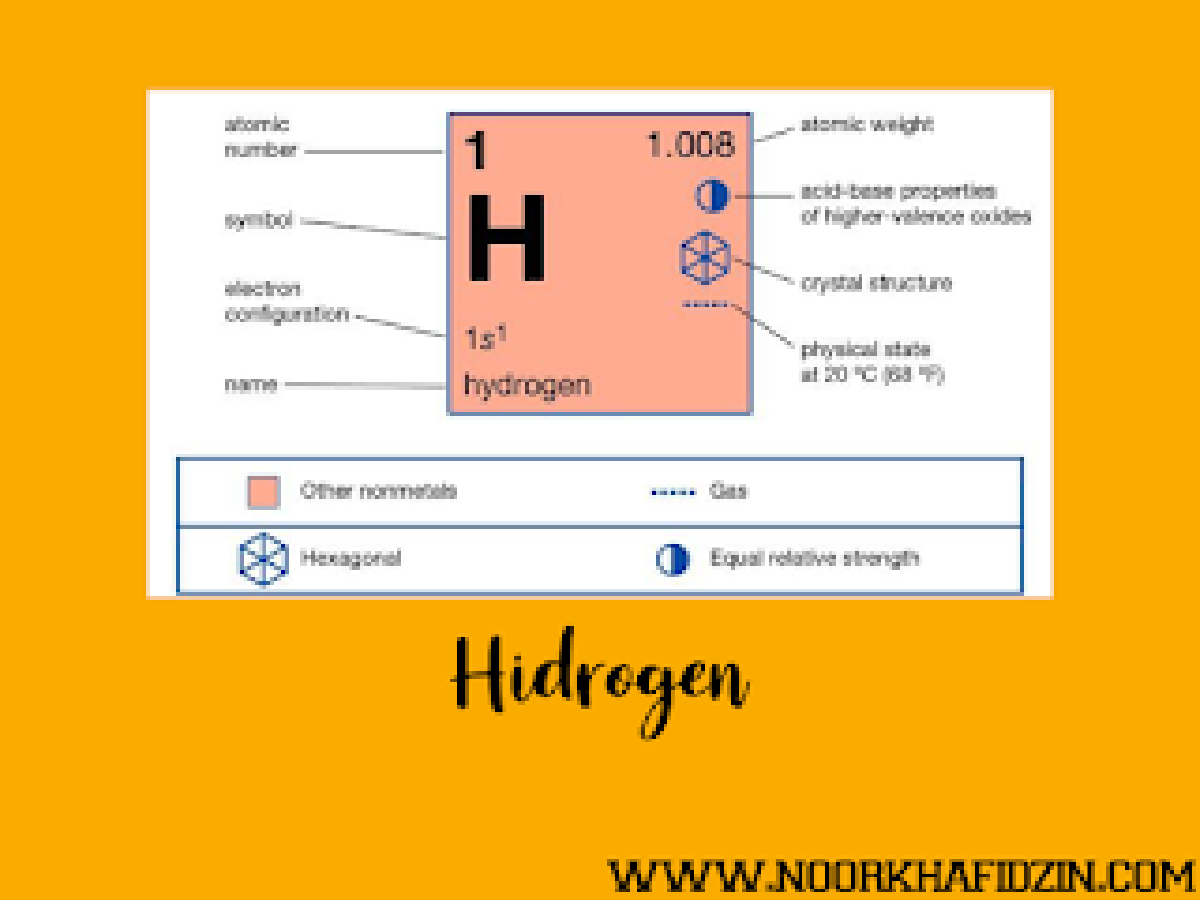
Kelimpahan Hidrogen di Alam #
Hidrogen merupakan unsur yang paling banyak ditemukan di alam semesta, yaitu sekitar 93%, karena bintang-bintang mengandung hidrogen sebagai bahan bakar untuk menghasilkan cahaya. Jumlah hidrogen di bumi sekitar 3%, atau 0,14% dari massa bumi, dalam bentuk senyawa anorganik (seperti air dan asam) maupun organik. Air mengandung sekitar 11% massa hidrogen karena molekulnya tersusun dari 2 atom hidrogen dan 1 atom oksigen.
Di alam, hidrogen memiliki 3 isotop, yaitu hidrogen (protium), deuterium, dan tritium. Perbandingannya adalah H : D : T = 10.000.000 : 2.000 : 1.
Reaksi-Reaksi pada Hidrogen #
Hidrogenolisis #
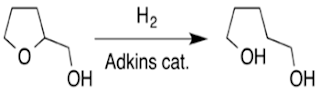
Hidrogenolisis adalah suatu reaksi kimia di mana suatu ikatan tunggal karbon-karbon atau karbon-heteroatom mengalami pembelahan atau lisis (pemecahan) oleh hidrogen. Heteroatom dapat bervariasi, tetapi umumnya berupa oksigen, nitrogen, atau belerang.
Contoh reaksi hidrogenolisis:
Hidrogenasi dan Dehidrogenasi #
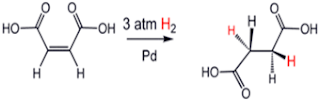
Hidrogenasi adalah suatu reaksi kimia yang melibatkan adisi atau penambahan molekul hidrogen pada suatu molekul. Reaksi ini biasanya terjadi pada molekul-molekul yang memiliki ikatan rangkap tidak jenuh, seperti alkena atau alkuna. Hidrogen akan teradisi pada ikatan rangkap molekul tersebut sehingga menghasilkan produk yang jenuh.
Contoh reaksi hidrogenasi:
Dehidrogenasi adalah reaksi kimia yang melibatkan penghilangan hidrogen dari molekul organik, dan merupakan kebalikan dari hidrogenasi. Dehidrogenasi merupakan reaksi penting karena mengubah alkana, yang relatif inert dan bernilai rendah, menjadi olefin yang reaktif dan lebih bernilai tinggi.
Contoh reaksi dehidrogenasi:
Hidrasi dan Dehidrasi #
Reaksi hidrasi adalah suatu reaksi kimia di mana suatu zat dikombinasikan dengan air. Dalam kimia organik, air ditambahkan pada substrat tak jenuh, biasanya berupa alkena atau alkuna.
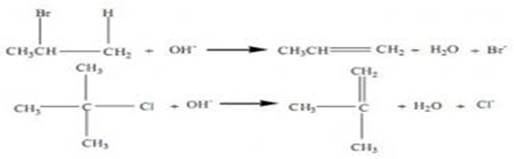
Reaksi dehidrasi dalam kimia didefinisikan sebagai reaksi yang melibatkan pelepasan air dari molekul yang bereaksi. Reaksi dehidrasi merupakan bagian dari reaksi eliminasi.
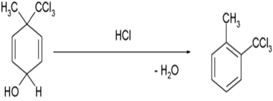
Contoh reaksi dehidrasi:
Contoh reaksi hidrasi:
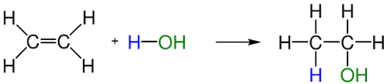
Sifat Fisika dan Sifat Kimia #
Sifat Fisika #
| Properti | Nilai |
|---|---|
| Nomor Atom | 1 |
| Massa Atom Relatif | 1 |
| Titik Leleh | -259,14 °C |
| Titik Didih | -252,87 °C |
| Warna | Tidak berwarna |
| Konfigurasi Elektron | 1s¹ |
| Energi Ionisasi | 1.312 kJ/mol |
| Afinitas Elektron | 72,77 kJ/mol |
| Keelektronegatifan | 2,20 |
| Jari-jari Ion | 1,46 Å |
| Jari-jari Atom | 0,37 Å |
| Massa Jenis | 0,0899 g/cm³ |
| Struktur Kristal | Heksagonal |
| Volume Atom | 14,10 cm³/mol |
| Entalpi Penguapan | 0,4581 kJ/mol |
| Entalpi Pembentukan | 0,0085 kJ/mol |
| Potensial Ionisasi | 13,598 V |
| Konduktivitas Panas | 0,1815 W m⁻¹ |
| Kapasitas Panas | 14,304 J g⁻¹ K⁻¹ |
| Golongan | Alkali |
| Wujud | Gas |
| Jenis Unsur | Nonlogam |
Sifat Kimia #
Hidrogen memiliki beberapa karakteristik kimia yang khas sebagai berikut.
1. Kehilangan elektron valensi 1s
Hal ini menghasilkan proton, H⁺. Ukurannya yang sangat kecil (r ~ 1,5 × 10⁻¹³ cm) relatif terhadap atom lain (r ~ 10⁻⁸ cm), serta muatannya yang kecil, menghasilkan kemampuan khas untuk mendistorsi awan elektron di sekeliling atom-atom lain. Proton tidak pernah hadir dalam bentuk bebas kecuali dalam berkas ion gas. Proton ini selalu bergabung dengan atom atau molekul lain. Meskipun ion hidrogen dalam air umumnya ditulis sebagai H⁺, sesungguhnya ia berbentuk H₃O⁺ atau H(H₂O)ₙ⁺.
2. Penambahan satu elektron
Atom H dapat memperoleh satu elektron dan membentuk ion hidrida, H⁻, dengan konfigurasi 1s² seperti helium. Ion ini hanya ada dalam kristal hidrida dari logam-logam elektropositif, seperti NaH dan CaH₂.
3. Pembentukan pasangan elektron bersama
Unsur nonlogam dan banyak logam dapat membentuk ikatan kovalen dengan hidrogen.
Kegunaan #
1. Pembuatan pupuk
Gas hidrogen digunakan sebagai bahan dalam proses pembuatan pupuk. Caranya adalah dengan mereaksikan hidrogen dengan senyawa nitrogen sehingga menghasilkan amonia (NH₃) yang menjadi bahan dasar pupuk nitrogen.
2. Penghilangan kandungan sulfur pada bahan bakar fosil
Proses penghilangan sulfur menggunakan hidrogen disebut hidrodesulfurisasi. Tujuannya adalah meminimalkan dampak polusi dari proses pembakaran bahan bakar. Jenis bahan bakar yang memanfaatkan proses ini antara lain bensin, solar, avtur, dan minyak tanah.
3. Bahan kimia organik
Gas hidrogen berperan dalam reaksi hidrogenasi untuk berbagai senyawa organik. Selain itu, hidrogen juga terlibat dalam reaksi kimia lain seperti reaksi asilasi.
4. Bahan bakar
Hidrogen dapat digunakan sebagai bahan bakar karena dapat terbakar dan menghasilkan air serta energi. Kelebihannya, satu satuan massa hidrogen yang dibakar menghasilkan sekitar tiga kali energi dibandingkan bensin dengan massa yang sama, serta menghasilkan emisi yang jauh lebih rendah.
5. Sintesis amonia
Hidrogen digunakan dalam proses Haber-Bosch untuk mensintesis amonia dari nitrogen dan hidrogen.
6. Pembuatan asam nitrat
Amonia yang dihasilkan dari proses Haber dioksidasi untuk menghasilkan NO sebagai bahan baku pembuatan asam nitrat.
7. Pembuatan margarin
Minyak nabati yang merupakan ester tidak jenuh diubah menjadi senyawa jenuh melalui reaksi hidrogenasi, menghasilkan margarin.
8. Cairan kriogenik
Hidrogen cair digunakan dalam berbagai aplikasi yang membutuhkan suhu sangat rendah.
9. Sintesis metanol
Hidrogen digunakan bersama karbon monoksida untuk mensintesis metanol secara industri.
10. Bahan bakar roket
Hidrogen cair digunakan sebagai bahan bakar roket karena sifatnya yang ringan dan memiliki nilai kalor yang tinggi.
11. Reduksi bijih tambang
Gas hidrogen digunakan sebagai agen pereduksi dalam pengolahan bijih logam.
12. Superkonduktor
Hidrogen cair digunakan dalam sistem superkonduktor karena titik didihnya yang mendekati nol absolut.
13. Fusi nuklir
Dua isotop hidrogen yang lebih berat, yaitu deuterium dan tritium, digunakan sebagai bahan bakar dalam reaksi fusi nuklir.